電池的工作原理
 24
24
 拍明芯城
拍明芯城

電池如何為我們的世界提供動力?查看更多 電池圖片.
電子庫存照片/思源想象一下這樣一個世界,所有用電的東西都必須插上電源。手電筒、助聽器、手機和其他便攜式設備將被拴在電源插座上,使它們變得笨拙和笨重。汽車不能通過簡單的轉動鑰匙來啟動;需要劇烈的起動才能使活塞移動。電線到處都是,造成安全隱患和難看的混亂。值得慶幸的是,電池為我們提供了一種移動電源,使許多現代便利成為可能。
雖然有許多不同類型的電池,但它們的基本概念保持不變。當設備連接到電池時,會發生產生電能的反應。這被稱為 電化學反應.意大利物理學家亞歷山德羅·沃爾塔伯爵(Count Alessandro Volta)于1799年首次發現了這一過程,當時他用金屬板和浸泡鹽水的紙板或紙創造了一個簡單的電池。從那時起,科學家們大大改進了Volta的原始設計,以制造由多種尺寸的材料制成的電池。
今天,電池就在我們身邊。它們一次為我們的腕表提供數月的動力。即使停電,他們也能保持我們的鬧鐘和電話正常工作。他們運行我們的 煙霧探測器、電動剃須刀、電鉆、 MP3播放器,恒溫器 - 等等。如果您在筆記本電腦上閱讀本文,或者 智能手機,您現在甚至可能正在使用電池!但是,由于這些便攜式電源組非常普遍,因此很容易將它們視為理所當然。本文將通過探索電池的歷史以及使它們工作的基本部件、反應和過程,讓您對電池有更深入的了解。因此,請剪斷電源線,然后單擊我們的信息指南,為您的電池知識充電。
電池歷史
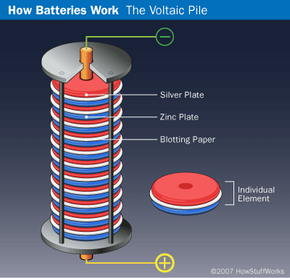
電池的歷史可以追溯到1800年。了解電池的歷史,并了解丹尼爾電池的構造方式。
電池存在的時間比您想象的要長。1938年,考古學家威廉·科尼格(Wilhelm Konig)在今伊拉克巴格達郊外的Khujut Rabu挖掘時發現了一些奇特的陶罐。這些罐子長約5英寸(12.7厘米),裝有一根用銅包裹的鐵棒,可追溯到公元前200年左右,測試表明這些容器曾經充滿醋或葡萄酒等酸性物質,導致Konig相信這些容器是古老的電池。自從這一發現以來,學者們已經制作了實際上能夠產生電荷的罐子的復制品。這些“巴格達電池”可能被用于宗教儀式、藥用目的,甚至電鍍。
1799年,意大利物理學家亞歷山德羅·沃爾塔(Alessandro Volta)創造了 第一塊電池 通過交替堆疊鋅、鹽水浸泡的粘貼板或布和銀層。這種安排稱為 伏打樁,不是第一個發電的設備,但它是第一個發出穩定、持久電流的設備。然而,沃爾特的發明有一些缺點。層可以堆疊的高度是有限的,因為堆的重量會將鹽水從粘貼板或布中擠出。金屬盤也容易迅速腐蝕,縮短電池的使用壽命。盡管有這些缺點,電動勢的SI單位現在被稱為伏特,以紀念沃爾特的成就。
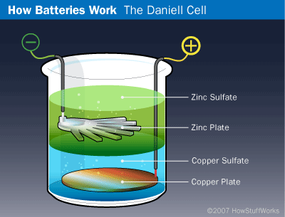
電池的歷史可以追溯到1800年。了解電池的歷史,并了解丹尼爾電池的構造方式。
電池技術的下一個突破出現在1836年,當時英國化學家約翰·弗雷德里克·丹尼爾發明了 丹尼爾細胞.在這個早期的電池中,將一塊銅板放在玻璃罐的底部,并將硫酸銅溶液倒在板上以將罐子裝滿一半。然后將鋅板掛在罐子里,加入硫酸鋅溶液。由于硫酸銅比硫酸鋅密度大,鋅溶液漂浮到銅溶液的頂部并包圍鋅板。連接到鋅板的導線代表負極端子,而從銅板引出的導線是正極端子。顯然,這種布置在手電筒中效果不佳,但對于固定應用,它工作得很好。事實上,在發電完善之前,丹尼爾電池是門鈴和電話的常用方式。
到1898年,哥倫比亞干電池成為第一個在美國銷售的商用電池。制造商National Carbon Company后來成為生產勁量品牌的Eveready電池公司
電池剖析
看看任何電池,你會注意到它有兩個 終端.一個端子標記為(+)或正,而另一個端子標記為(-)或負極。在普通手電筒電池中,如 AA、C 或 D 電池,端子位于末端。然而,在 9 伏或汽車電池上,端子彼此相鄰地位于設備頂部。如果在兩個端子之間連接一根導線,電子將以最快的速度從負端流向正端。這會很快磨損電池,也可能很危險,尤其是在較大的電池上。要正確利用電池產生的電荷,必須將其連接到 負荷.負載可能類似于 電燈泡、電機或電子電路,如 收音機.
電池的內部工作原理通常安裝在金屬或塑料外殼內。在這種情況下,有一個 陰極,連接到正極,以及 陽極,連接到負極端子。這些組件,通常稱為 電極,占據電池中的大部分空間,是發生化學反應的地方。一個 分隔符 在陰極和陽極之間形成屏障,防止電極接觸,同時允許電荷在它們之間自由流動。允許電荷在陰極和陽極之間流動的介質稱為 電解質.最后, 收藏家 將電荷傳導到電池外部并通過負載。
在下一頁中,我們將探討陰極、陽極、電解質、隔板和集電極如何協同工作以產生電流并保持便攜式設備運行良好。
電池反應和化學
當您將電池放入手電筒、遙控器或其他無線設備時,電池內部會發生很多事情。雖然它們發電的過程因電池而異,但基本思想保持不變。
當加載完成 電路 在兩個端子之間,電池通過陽極、陰極和電解質之間的一系列電磁反應發電。陽極經歷 氧化反應 其中兩個或更多 離子 來自電解質的(帶電原子或分子)與陽極結合,產生化合物并釋放一個或多個電子。同時,陰極經過 還原反應 其中陰極物質、離子和自由電子也結合形成化合物。雖然這個動作聽起來很復雜,但實際上非常簡單:陽極中的反應產生電子,陰極中的反應吸收它們。凈產品是電力。電池將繼續發電,直到一個或兩個電極耗盡反應發生所需的物質。
現代電池使用各種化學物質來為其反應提供動力。常見的電池化學成分包括:
鋅碳電池:鋅碳化學在許多廉價的AAA,AA,C和D干電池中很常見。陽極是 鋅,陰極為二氧化錳,電解質為氯化銨或氯化鋅。
堿性電池:這種化學成分在AA,C和D干電池中也很常見。陰極由二氧化錳混合物組成,而陽極是鋅粉。它的名字來自氫氧化鉀電解質,這是一種堿性物質。
鋰離子電池(可充電):鋰化學通常用于高性能設備,如手機、數碼相機甚至電動汽車。鋰電池中使用了多種物質,但常見的組合是鈷酸鋰陰極和碳陽極。
鉛酸電池(可充電):這是典型汽車電池中使用的化學成分。電極通常由二氧化鉛和金屬鉛制成,而電解質是硫酸溶液。
了解這些反應的最好方法是親眼看看。轉到下一頁進行一些動手電池實驗。
由空氣提供動力?
研究人員目前正在開發一種電池,其中的電極將是鋰,令人驚訝的是,空氣中的氧氣。這樣的進步將大大減輕電池重量,并且可能擁有傳統鋰離子電池能量的5到10倍。雖然這項技術仍有許多障礙需要克服,但它有朝一日可能會徹底改變電動汽車行業。
電池實驗:伏打樁
如果你想了解更多關于電池中發生的電化學反應的信息,你實際上可以使用簡單的家用材料自己建造一個。在開始之前你應該買的一件事是便宜的($10到$ 20) 伏特歐姆表 在您當地的電子產品或五金店。確保測量儀可以讀取低電壓(在 1 伏范圍內)和低電流(在 5 到 10 毫安范圍內)。有了這個設備,您將能夠準確地看到電池的性能。
您可以使用四分之一,箔紙,吸墨紙,蘋果醋和鹽創建自己的伏打樁。將箔紙和吸墨紙切成圓圈,然后將吸墨紙浸泡在蘋果醋和鹽的混合物中。使用遮蔽膠帶,附加 銅 連接到其中一個鋁箔盤。現在按此順序堆疊材料:箔、紙、四分之一、箔、紙、四分之一,依此類推,直到您重復該模式 10 次。一旦最后一枚硬幣在堆棧上,用遮蔽膠帶將電線連接到它。最后,將兩根電線的自由端連接到 發光二極管,應該亮起。在這個實驗中,四分之一中的銅是陰極,箔是陽極,蘋果醋鹽溶液是電解質,吸墨紙是分離器。
自制電池也可以由銅線、回形針和檸檬制成。首先,剪一根短銅線,拉直回形針。使用砂紙磨平任一金屬末端的任何粗糙部件。接下來,通過在桌子上滾動檸檬來輕輕擠壓檸檬,但要注意不要破皮。將銅線和回形針推入檸檬中,確保它們盡可能靠近而不會實際接觸。最后,將伏歐表連接到回形針和銅線的末端,看看電池產生的電壓和電流。
到目前為止,您應該已經熟悉電池放電的基本原理。
加語S vs. 電動
盡管存在種種缺點,但汽油仍然是汽車的主要燃料。為什么電池沒有流行起來?最大的問題之一是能量密度 - 燃料可以存儲的能量與其重量的關系,以每公斤瓦特小時為單位。汽油的能量密度約為每公斤13,000瓦時,而目前最好的鋰離子電池每公斤只能容納200瓦時
可充電電池
隨著便攜式設備的興起,例如 筆記本 電腦, 手機, MP3播放器 和無繩電動工具,近年來對可充電電池的需求大幅增長。可充電電池自1859年以來一直存在,當時法國物理學家加斯頓·普蘭特(Gaston Plante)發明了鉛酸電池。普蘭特電池具有鉛陽極、二氧化鉛陰極和硫酸電解質,是現代汽車電池的前身。
不可充電電池,或 原代細胞和可充電電池,或 二次細胞,以完全相同的方式產生電流:通過涉及陽極、陰極和電解質的電化學反應。然而,在可充電電池中,反應是可逆的。當來自外部來源的電能施加到二次電池時,放電過程中發生的負電子流到正電子流被逆轉,電池的電荷被恢復。當今市場上最常見的可充電電池是 鋰離子 (獅子),雖然 鎳氫 (鎳氫)和 鎳鎘 (NiCd)電池也曾經非常普遍。
當談到可充電電池時,并非所有電池都是平等的。鎳鎘電池是首批廣泛使用的二次電池之一,但它們遇到了一個不方便的問題,稱為 記憶效應.基本上,如果這些電池每次使用時都沒有完全放電,它們很快就會失去容量。鎳鎘電池在很大程度上被淘汰,取而代之的是鎳氫電池。這些二級細胞具有更高的容量,并且僅受記憶效應的影響很小,但它們的保質期不是很好。與鎳氫電池一樣,LiOn電池的使用壽命很長,但它們可以更好地保持電荷,在更高的電壓下運行,并且采用更小,更輕的包裝。基本上,現在制造的所有高質量便攜式技術都利用了這項技術。然而,LiOn電池目前沒有標準尺寸,如AAA,AA,C或D,而且它們比舊的同類產品貴得多。
使用鎳鎘和鎳氫電池,充電可能很棘手。您必須小心不要過度充電,因為這可能會導致容量下降。為了防止這種情況發生,一些充電器會切換到涓流充電,或者在充電完成后直接關閉。鎳鎘和鎳氫電池也必須修復,這意味著您應該每隔一段時間完全放電并再次充電,以盡量減少容量損失。另一方面,LiOn電池具有復雜的充電器,可防止過度充電,并且永遠不需要翻新。
即使是可充電電池最終也會耗盡,盡管可能需要數百次充電才能發生這種情況。當它們最終分發時,請務必將它們丟棄在回收設施中。
接下來,我們來看看電池排列。
電池排列和電源
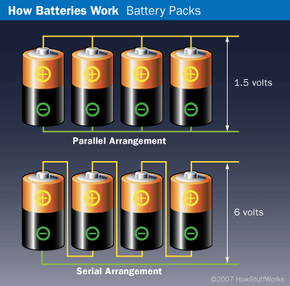
電池排列決定電壓和電流。查看串行電池排列、并聯排列以及最大電流是多少。
在許多使用電池的設備中 - 例如便攜式 收音機 和手電筒 - 你一次只使用一個細胞。您通常將它們組合在一起 串行 安排 以增加 電壓 或在 平行排列 以增加 當前.該圖顯示了這兩種安排。
上圖顯示了一個 平行排列.并聯的四個電池將共同產生一個電池的電壓,但它們提供的電流將是單個電池的四倍。 當前 是電荷通過的速率 電路,并以安培為單位。電池的額定值為安培小時,或者,對于較小的家用電池,則為毫安小時 (mAH)。額定功率為 500 毫安小時的典型家用電池應該能夠為負載提供 500 毫安的電流一小時。您可以通過許多不同的方式對毫安小時額定值進行切片和切塊。一個 500 毫安小時的電池也可以產生 5 毫安的 100 小時,10 毫安的 50 小時,或者理論上,1,000 毫安的 30 分鐘。一般來說,安培小時額定值較高的電池具有更大的容量。
下圖描繪了一個 串行排列.串聯的四個電池將共同產生一個電池的電流,但它們提供的電壓將是單個電池的四倍。 電壓 是每單位電荷能量的量度,以伏特為單位。在電池中,電壓決定了電子通過電路的強度,就像壓力決定了水通過軟管的強度一樣。大多數 AAA、AA、C 和 D 電池的電壓約為 1.5 伏。
想象一下,圖中所示的電池額定電壓為 1.5 伏,500 毫安時。四個并聯排列的電池將在 2,000 毫安時時產生 1.5 伏電壓。串聯排列的四個電池將在 6 毫安時產生 500 伏的電壓。
自伏打樁時代以來,電池技術取得了長足的進步。這些發展清楚地反映在我們快節奏的便攜式世界中,它比以往任何時候都更加依賴電池提供的便攜式電源。人們只能想象下一代更小、更強大、更持久的電池將帶來什么。
電池常見問題
什么是電池能量?
電池中的能量以瓦特小時(符號 Wh)表示,即電池提供的電壓 (V) 乘以它在給定時間(通常以小時為單位)內可以提供的電流 (安培)。
電池有哪些不同類型?
常見的電池化學成分(或類型)包括:鋅碳、堿性、鋰離子(可充電)和鉛酸(也可充電)。研究人員目前正在開發一種“空氣”電池,其中電極將是來自空氣中的鋰和氧氣。
汽車電池多少錢?
預計為典型的汽車電池支付 50 至 120 美元,為具有更長保修期、更好的寒冷天氣性能或用于豪華車的電池支付 90-200 美元或更多。
電池的能量來源是什么?
電池通過電化學反應產生能量。簡單地說,陽極中的反應產生電子,陰極中的反應吸收它們。凈產品是電力。
充電電池是什么類型?
市場上最常見的可充電電池是鋰離子(LiOn),盡管鎳氫(NiMH)和鎳鎘(NiCd)電池過去也很普遍。
責任編輯:David
【免責聲明】
1、本文內容、數據、圖表等來源于網絡引用或其他公開資料,版權歸屬原作者、原發表出處。若版權所有方對本文的引用持有異議,請聯系拍明芯城(marketing@iczoom.com),本方將及時處理。
2、本文的引用僅供讀者交流學習使用,不涉及商業目的。
3、本文內容僅代表作者觀點,拍明芯城不對內容的準確性、可靠性或完整性提供明示或暗示的保證。讀者閱讀本文后做出的決定或行為,是基于自主意愿和獨立判斷做出的,請讀者明確相關結果。
4、如需轉載本方擁有版權的文章,請聯系拍明芯城(marketing@iczoom.com)注明“轉載原因”。未經允許私自轉載拍明芯城將保留追究其法律責任的權利。
拍明芯城擁有對此聲明的最終解釋權。




 產品分類
產品分類























 2012- 2022 拍明芯城ICZOOM.com 版權所有 客服熱線:400-693-8369 (9:00-18:00)
2012- 2022 拍明芯城ICZOOM.com 版權所有 客服熱線:400-693-8369 (9:00-18:00)


